El mantenimiento del volumen total y la composición de los líquidos corporales es relativamente constante en la mayoría de procesos fisiológicos, algo esencial para la homeostasis. No obstante, algunos de los problemas más importantes que aparecen en la medicina clínica se deben a anomalías en los sistemas de control que mantienen dicha constancia. En este capítulo analizamos la regulación global del volumen del líquido corporal, el control de los constituyentes del líquido extracelular, el control del intercambio de líquido entre los compartimientos extracelular e intracelular y la regulación del equilibrio acidobásico.
LA INGESTIÓN Y LA PÉRDIDA DE LÍQUIDO ESTÁN EQUILIBRADAS DURANTE LAS SITUACIONES ESTABLES

La ingestión total de agua y electrólitos debe coincidir minuciosamente con iguales pérdidas corporales para prevenir que las concentraciones de volúmenes y electrólitos aumenten o disminuyan.
En la mayoría de los casos, la forma más importante de controlar las pérdidas es alterando la excreción renal. El volumen de orina puede ser de tan solo 0,5 l/día en una persona deshidratada, o hasta de 201/día en una persona que ha bebido grandes cantidades de líquidos. Esta capacidad de los riñones para ajustar las pérdidas hasta ese extremo para coincidir con la ingesta también afecta a los electrólitos corporales, como el sodio, el cloruro y el potasio.
EL LÍQUIDO CORPORAL SE DISTRIBUYE ENTRE EL LÍQUIDO EXTRACELULAR Y EL LÍQUIDO INTRACELULAR

En el hombre adulto medio de 70 kg, el agua corporal total supone alrededor del 60% del peso corporal o unos 42 l. Debido a que las mujeres tienen normalmente un mayor porcentaje de grasa corporal que los hombres, sus promedios totales de agua en el organismo son aproximadamente de un 50% del peso corporal. En bebés prematuros y neo natos, el agua total en el organismo está situada en el 70- 75% del peso corporal. Así, cuando se analicen los compartimientos «medios» de líquido corporal, deberemos tener en cuenta que existen variaciones dependiendo de la edad, el sexo y el porcentaje de grasa corporal.
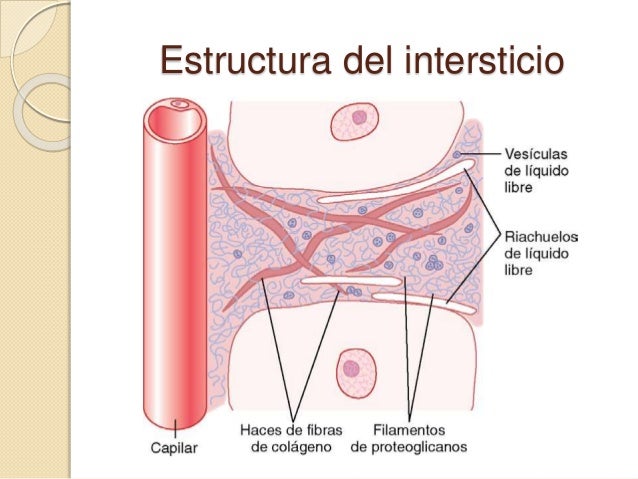
El líquido corporal total se distribuye en dos compartimientos principales: 1) el líquido intracelular, que supone el 40% del peso corporal o 28 1 en un hombre que pese 70 kg, y 2) el líquido extracelular, que supone el 20% del peso corporal, o 141 en un hombre de 70 kg. Los dos compartimientos más grandes del líquido extracelular son el líquido intersticial, que supone unas tres cuartas partes del líquido extracelular, y el plasma, que supone casi una cuarta parte del líquido extracelular, o unos 3 l. El plasma es la parte no celular de la sangre que intercambia sustancias continuamente con el líquido intersticial a través de los poros de las membranas capilares.
La sangre contiene líquido extracelular e intracelular.
El volumen sanguíneo medio de los adultos es del 8% del peso corporal, o unos 5 l. Alrededor del 60% de la sangre es plasma, y alrededor del 40%, eritrocitos. El hematocrito, la fracción de la sangre compuesta de eritrocitos, es normalmente de alrededor de 0,42 y, en las mujeres, de alrededor de 0,38. En la anemia grave, el hematocrito puede reducirse hasta tan solo 0,1, un valor que apenas es suficiente para mantener la vida. Cuando hay una producción excesiva de eritrocitos, lo que provoca una policitemia, el hematocrito puede aumentar hasta 0,65.
Los constituyentes de los líquidos extracelular e intracelular son diferentes.

El plasma y el líquido intersticial están separados por membranas capilares muy permeables, por lo que su composición iónica es similar. La diferencia más importante entre estos dos compartimientos es la mayor concentración de proteínas en el plasma; debido a que los capilares tienen una permeabilidad baja a las proteínas plasmáticas, solo pequeñas cantidades de proteínas pasan a los espacios intersticiales en la mayoría de los tejidos. El líquido intracelular está separado del líquido extracelular por una membrana celular muy permeable al agua, pero no a la mayoría de los electrólitos del cuerpo. Por este motivo, la concentración de agua y la osmolaridad de los líquidos intracelular y extracelular son aproximadamente iguales en condiciones de equilibrio, aunque las concentraciones de varios solutos son muy diferentes en estos compartimientos líquidos.
EL PRINCIPIO DE DILUCIÓN DEL INDICADOR PUEDE MEDIR LOS VOLÚMENES DE LOS COMPARTIMIENTOS HÍDRICOS DEL CUERPO
El volumen de un líquido en un compartimiento del cuerpo puede medirse colocando una sustancia indicadora en el compartimiento, permitiendo que se disperse de forma homogénea y, después, analizando la proporción en que se ha diluido. Este método se basa en la suposición de que la canti- t dad total de sustancia que se mantiene en el compartimiento después de la dispersión es la misma que la cantidad total de sustancia que fue inyectada en el compartimiento. Por ·s tanto, cuando se inyecta una pequeña cantidad de sustancia, contenida en la jeringa A, en el compartimiento B y se deja que esa sustancia se disperse a través del compartimiento hasta que se mezcle en concentraciones iguales en todas las áreas, se puede aplicar la siguiente expresión:
VoIumen B= (Volumen A) (Concentración A) / Concentración B
Este método puede usarse para medir el volumen de prácticamente cualquier compartimiento corporal, si: 1) se conoce la cantidad total de indicador inyectado en el compartimiento (el numerador de la ecuación); 2) se conoce la concentración del indicador en el compartimiento; 3) el indicador se dispersa homogéneamente por todo el compartimiento, y 4) el indicador solo se dispersa en el compartimiento que se está midiendo.
Los volúmenes de los dos compartimientos, los líquidos intersticiales intracelular y extracelular, no pueden medirse directamente, por lo que se calculan a partir de los valores de los volúmenes de otros líquidos corporales.
LA DISTRIBUCIÓN DEL LÍQUIDO ENTRE LOS COMPARTIMIENTOS INTRACELULAR Y EXTRACELULAR SE DETERMINA, PRINCIPALMENTE, POR EL EFECTO OSMÓTICO DE LOS ELECTRÓLITOS A TRAVÉS DE LA MEMBRANA CELULAR

Dado que las membranas celulares son muy permeables al agua, pero relativamente impermeables incluso a iones pequeños como el sodio y el cloro, la distribución de líquidos entre los compartimientos intracelular y extracelular está determinada, principalmente, por los efectos osmóticos de dichos iones. Los principios básicos de la ósmosis y la presión osmótica se presentan en el capítulo 4. Por tanto, en esta sección solo se comentarán los principios más importantes aplicables a la regulación del volumen.
La ósmosis es la difusión neta de agua a través de una
membrana con una permeabilidad selectiva.
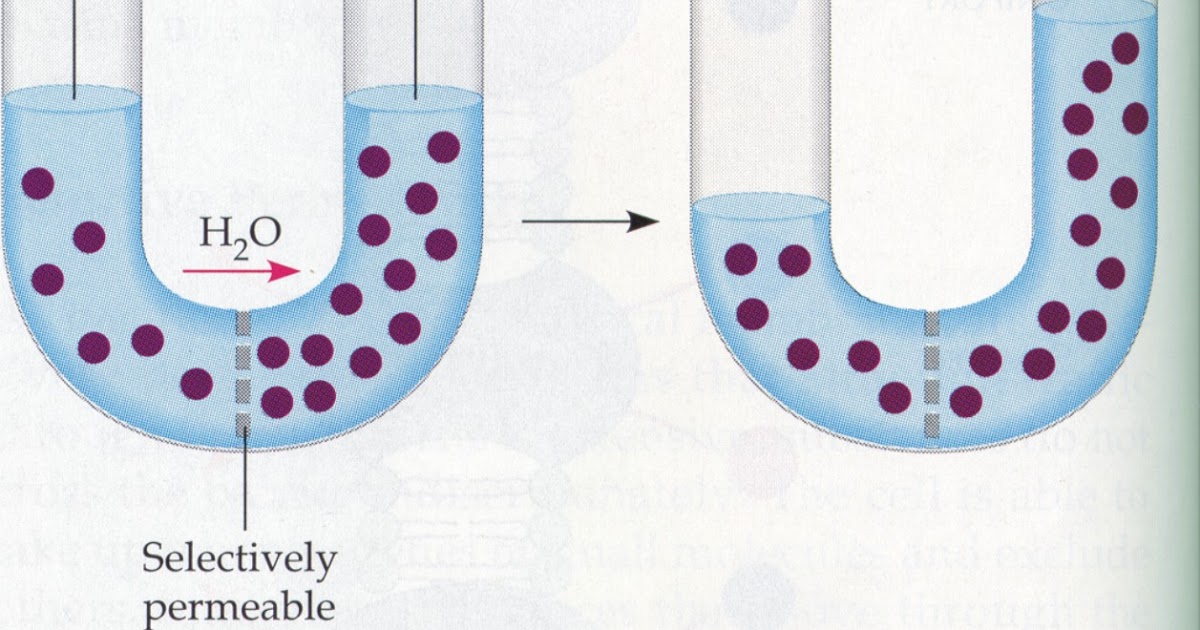
Cuando se añade un soluto al agua pura, se reduce la concentración de agua en la mezcla y el agua se desplaza hacia la región con concentración alta de solutos. El término de concentración que se utiliza para medir el número total de partículas de soluto en la solución es el osmol: 1 osmol es igual a 1 mol (6,02 X 1023) de partículas de soluto. En las soluciones biológicas, se utiliza habitualmente el milíosmol (mOsm), que es igual a 1/1.000 osmoles. La concentración osmolar de una solución se denomina osmolalidad cuando la concentración se expresa en osmoles por kilogramo de agua; se llama osmolaridad cuando se expresa en osmoles por litro de solución. La cantidad de presión necesaria para evitar la ósmosis de agua a través de una membrana semipermeable se denomina presión osmótica. Expresada matemáticamente, la presión osmótica (x) es directamente proporcional a la concentración de partículas osmóticamente activas en esa solución.
n = CRT
donde C es la concentración de solutos en osmoles por litro, Res la constante de gas ideal y Tes la temperatura absoluta en grados Kelvin. Si 7t se expresa en milímetros de mercurio (la unidad de presión utilizada habitualmente para los líquidos biológicos), se calcula un valor de rt de 19,3 mmHg para una solución con una osmolaridad de 1 mOsm/l. Por tanto, por cada miliosmol de gradiente de concentración de soluto que atraviese la membrana celular, se requiere una fuerza de 19,3 mmHg para evitar la difusión del agua a través de la membrana. Por tanto, diferencias muy pequeñas de la concentración de solutos en la membrana celular provocan una ósmosis rápida de agua.
Líquidos isotónicos, hipotónicos e hipertónicos.
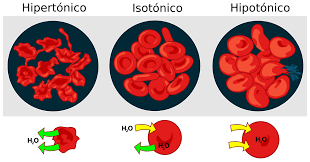
Se dice que una solución es isotónica si no se desarrolla ninguna fuerza osmótica a través de la membrana celular cuando se introduce una célula normal en la solución. Una solución isotónica tiene la misma osmolaridad que la célula, y las r,l células no encogen ni se hinchan cuando se introducen en la solución. Ejemplos de soluciones isotónicas son la solució de cloruro de sodio al 0,9% o la solución de glucosa al 5%. t Se dice que una solución es hipertónica cuando contiene una concentración mayor de sustancias osmóticas que la célula. En este caso, se desarrolla una fuerza osmótica que ·s hace que el agua salga de la célula hacia la solución, reduciendo el volumen del líquido intracelular y aumentando la concentración del -líquido intracelular.
Se dice que una solución es hipotónica si la concentración osmótica de sustancias en la solución es menor que la concentración de la célula. La fuerza osmótica se desarrolla inmediatamente, cuando la célula se expone a la solución, haciendo que el agua entre en la célula por ósmosis hasta que el líquido intracelular tenga la misma concentración que el líquido extracelular, o hasta que la célula estalle como consecuencia de una tumefacción excesiva.
VOLUMEN Y OSMOLALIDAD DE LOS LÍQUIDOS INTRACELULAR Y EXTRACELULAR EN ESTADOS ANORMALES
Algunos de los factores que pueden hacer que los volúmenes extracelular e intracelular cambien significativamente son la ingestión de grandes cantidades de agua, la deshidratación, la infusión intravenosa de diferentes tipos de soluciones, la pérdida de grandes cantidades de líquido a través del aparato digestivo y la pérdida de cantidades anómalas de líquido a través del sudor o de los riñones. Uno puede calcular los cambios en los volúmenes de líquido extracelular e intracelular y los tipos de tratamiento que deben instituirse si se tienen en mente los siguientes principios básicos:
– El agua se mueve rápidamente a través de las membranas celulares; por tanto, las osmolaridades de los líquidos intracelular y extracelular permanecen casi exactamente
iguales, excepto durante unos minutos después de un cambio en uno de los compartimientos.
– Las membranas celulares son casi completamente impermeables a la mayoría de solutos; así, el número de osmoles en el líquido extracelular e intracelular permanece relativamente constante salvo que se añadan o retiren solutos en el compartimiento extracelular.
Efecto de la adición de una solución salina isotónica, hipertónica o hipotónica al líquido extra celular

Si se añade una solución salina isotónica al compartimiento líquido extracelular, la osmolaridad del líquido extracelular no cambia, luego no se produce ninguna ósmosis a través de las membranas celulares. El único efecto es un aumento del volumen de líquido extra celular. El sodio y el cloro permanecen en gran medida en el líquido extracelular porque las membranas celulares se comportan como si fueran casi impermeables al cloruro de sodio. Si se añade una solución hipertánica al líquido extracelular, la osmolaridad extracelular aumenta y provoca la ósmosis del agua fuera de las células hacia el compartimiento extracelular. El efecto neto es un aumento del volumen extracelular (mayor que el volumen de líquido añadido), una reducción del volumen intracelular y un aumento de la osmolaridad en los dos compartimientos. Si se añade una solución hipotónica al líquido extracelular, la osmolaridad del líquido extracelular disminuye y parte del agua extracelular difunde al interior de las células hasta que los compartimientos extracelular e intracelular tienen la misma osmolaridad. Los volúmenes extracelular e intracelular aumentan al añadir líquido hipotónico, aunque el volumen intracelular lo hace en mayor grado.
EDEMA: EXCESO DE LÍQUIDO EN LOS TEJIDOS

Edema intracelular: aumento del líquido
intracelular
Tres procesos causan especialmente tumefacción intracelular: 1) la hiponatremia; 2) la depresión de los sistemas metabólicos de los tejidos, y 3) la falta de una nutriciócelular adecuada. Cuando los sistemas metabólicos de la célula están deprimidos o reciben nutrición inadecuada, los iones sodio que normalmente se filtran hacia el interior de las células ya no pueden salir bombeados de ellas y el exceso de sodio intracelular causas por ósmosis el paso del agua a interior de las células.
El edema intracelular también puede producirse en lo tejidos inflamados. La inflamación suele aumentar la permeabilidad de las membranas celulares, lo que permite al sodio y a otros iones difundir hacia el interior de la célula, con la posterior entrada del agua por ósmosis al interior de las células.
Edema extracelular: aumento del líquido
en los espacios intersticiales
Hay dos causas generales de edema extracelular: 1) la fuga anormal de líquido del plasma hacia los espacios intersticiales a través de los capilares, y 2) la imposibilidad de los linfáticos de devolver el líquido a la sangre desde el intersticio, lo que a menudo se conoce por linfedema.
Factores que pueden aumentar la filtración capilar y provocan edema del líquido intersticial.
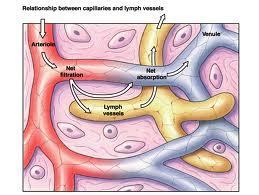
Para conocer las causas de la filtración capilar excesiva resulta útil revisar los determinantes de la filtración capilar expuestos en el capítulo 16. La filtración capilar puede expresarse mediante la siguiente fórmula matemática: Filtración = Kt X (Pe – P¡f – 1tc + 7t¡¡) donde K, es el coeficiente de filtración capilar (el producto de la permeabilidad y el área superficial de los capilares), P¡f es la presión hidrostática del líquido intersticial, 1tc es la presión coloidosmótica del plasma capilar y 1t¡f es la presión coloidosmótica del líquido intersticial. A partir de esta ecuación, podemos ver que cualquiera de los siguientes cambios puede aumentar la filtración capilar:
- Aumento del coeficiente de filtración capilar, que permite una mayor fuga de líquidos y proteínas plasmáticas a través de las membranas capilares como consecuencia, por ejemplo, de reacciones alérgicas, infecciones bacterianas y sustancias tóxicas que lesionan las membranas capilares y aumentan su permeabilidad a las proteínas plasmáticas.
- Aumento de la presión hidrostática capilar, que puede ser consecuencia de la obstrucción venosa, de un flujo excesivo de sangre desde las arterias hacia los capilares o del fracaso de la función de bomba del corazón para manejar con rapidez el aferente venoso (insuficiencia cardíaca).
- Reducción de la presión coloidosmótica del plasma, que puede ser consecuencia del fracaso del hígado para producir cantidades suficientes de proteínas plasmáticas (cirrosis), de la pérdida de grandes cantidades de proteínas en la orina en algunas enfermedades renales (síndrome nefrótico) o de la pérdida de grandes cantidades
de proteínas a través de las áreas de la piel quemadas u otras lesiones con denudación.
- Aumento de la presión coloidosmática en el líquido intersticial, que extrae líquido del plasma hacia los espacios tisulares. Esta situación es más frecuente como consecuencia del bloqueo linfático, que previene el retorno de las proteínas desde los espacios intersticiales hacia la sangre (como se comenta en las secciones siguientes).
La obstrucción linfática causa edema.

Cuando se produce una obstrucción, el edema puede ser especialmente intenso porque no hay otra forma de extraer las proteínas plasmáticas que salen al intersticio. El aumento de la concentración de proteínas eleva la presión coloidosmótica del líquido intersticial, lo que arrastra incluso más líquido fuera de los capilares. La obstrucción del flujo linfático puede ser especialmente intensa con las infecciones de los ganglios linfáticos, como ocurre en la infección por los nematodos filarias. Los vasos linfáticos también pueden obstruirse en ciertos tipos de cáncer o después de una cirugía en que se eliminen u obstruyan.
Mecanismos de seguridad que normalmente impiden el edema

Aunque muchos trastornos pueden causar acumulación de fluidos en los espacios intersticiales, la anomalía debe ser acentuada antes de que aparezca un edema clínicamente
significativo. Tres mecanismos de seguridad importantes impiden normalmente la acumulación de líquido en los espacios intersticiales:
– La distensibilidad de los tejidos es baja mientras la presión hidrostática del líquido intersticial es negativa. Una baja distensibilidad (definida como el cambio del volumen por milímetro de mercurio que cambie la presión) significa que pequeños aumentos del volumen
del líquido intersticial se asocian a aumentos relativamente importantes de la presión hidrostática en el líquido intersticial. Cuando aumenta el volumen del líquido intersticial, la presión hidrostática también aumenta mucho, oponiéndose a una filtración capilar excesiva.
El factor de seguridad que protege frente al edema para este efecto es de unos 3 mmHg en muchos tejidos como la piel.
– El flujo de linfa puede aumentar 10-50 veces. Los vasos linfáticos transportan grandes cantidades de líquido y proteínas en respuesta a un aumento de la filtración capilar. Se ha calculado que el mecanismo de seguridad del aumento del flujo linfático es de unos 7 mmHg. – Se produce un «lavado» de las proteínas del líquido al intersticio a medida que aumenta el flujo de linfa. La presión en el líquido intersticial aumenta a medida que ·s aumenta la cantidad de líquido filtrado hacia el intersticio, aumentando el flujo linfático. Este efecto reduce la concentración de proteínas en el intersticio debido a la eliminación de una mayor cantidad de proteínas que pueden filtrarse desde los capilares. El descenso de la concentración de proteínas en el líquido tisular reduce la fuerza de filtración neta a través de los capilares y tiende a evitar una mayor acumulación de líquido. Se ha calculado que el factor de seguridad para este efecto es de unos 7 mmHg en la mayoría de los tejidos.
Cuando se combinan todos estos factores de seguridad, el factor de seguridad total que protege frente al edema es de 17 mmHg. Por tanto, en teoría, la presión capilar en los tejidos periféricos podría aumentar 17 mmHg antes de que se produzca un edema importante.





































/vascular-system-veins-56c87fa03df78cfb378b3e7c.jpg)